Sisältö
Vaikka saman elementin kaikki atomit sisältävät saman määrän protoneja, neutronien lukumäärä voi vaihdella. Sen tietäminen, kuinka monta neutronia tietyllä atomilla on, voi auttaa sinua selvittämään, onko partikkeli säännöllinen siinä elementissä vai isotoopissa, jossa on enemmän tai vähemmän neutroneja. Neutronien lukumäärän määrittäminen atomissa on melko yksinkertaista eikä vaadi mitään kokeita. Noudata näitä ohjeita jaksollisen taulukon avulla laskeaksesi normaalin atomin tai isotoopin neutronien lukumäärän.
Askeleet
Menetelmä 1/2: neutraalien lukumäärän löytäminen yhteisestä atomista
Etsi elementti jaksotaulusta. Katsotaan tässä esimerkissä kuudennella rivillä olevaa käyttöjärjestelmää (Os) ylhäältä alas.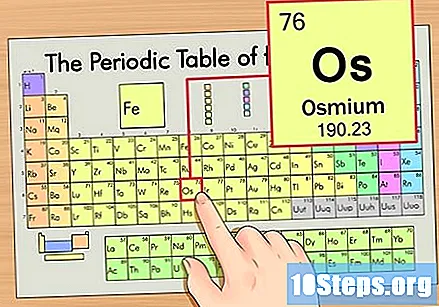
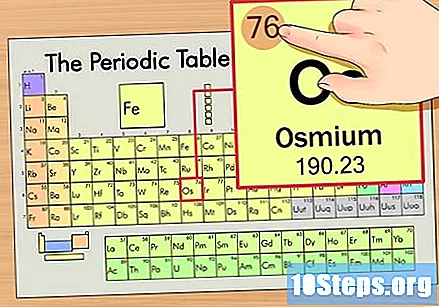
Etsi alkuaineen atominumero. Tämä on yleensä tietyn elementin näkyvin numero ja on yleensä sen symbolin yläpuolella (käyttämässämme taulukossa ei itse asiassa ole muita numeroita). Atomiluku on protonien lukumäärä kyseisen elementin yhdessä atomissa. Os-lukumäärä on 76, mikä tarkoittaa, että Osmium-atomilla on 76 protonia.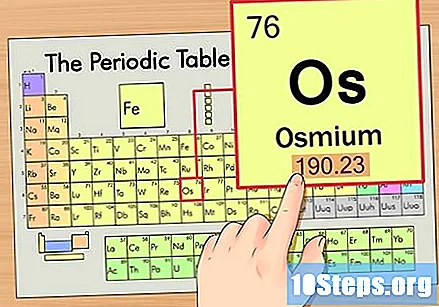
Etsi alkuaineen atomipaino. Tämä luku löytyy yleensä atomisymbolin alapuolelta. Huomaa, että tämän esimerkin taulukko perustuu vain atominumeroon eikä siinä luetelta atomipainoa. Näin ei aina ole. Osmiumin atomipaino on 190,23.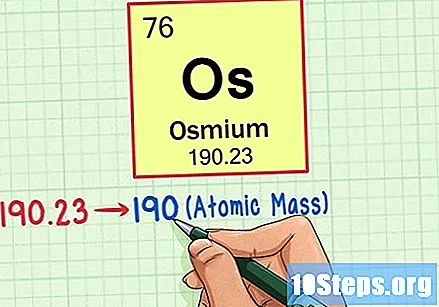
Pyöristä atomipaino lähimpään kokonaislukuun löytääksesi atomimassan. Esimerkissämme 190,23 pyöristettäisiin 190: ksi, jolloin atomin massa 190 olisi Osmiumin suhteen.- Atomimassa on elementin isotooppien keskiarvo. Siksi se ei yleensä ole kokonaisluku.
Vähennä atominumero atomimassasta. Koska valtaosa atomin massasta löytyy sen protoneista ja neutraaleista, vähentämällä protonien lukumäärä (eli atominumero) atomimassasta saadaan numero laskettu neutronien määrä atomissa. Desimaalipilkun jälkeinen lukumäärä edustaa yleensä erittäin pientä elektronien massaa atomissa. Esimerkissämme tämä on: 190 (atomimassa) - 76 (protonien lukumäärä) = 114 (neutronien lukumäärä).
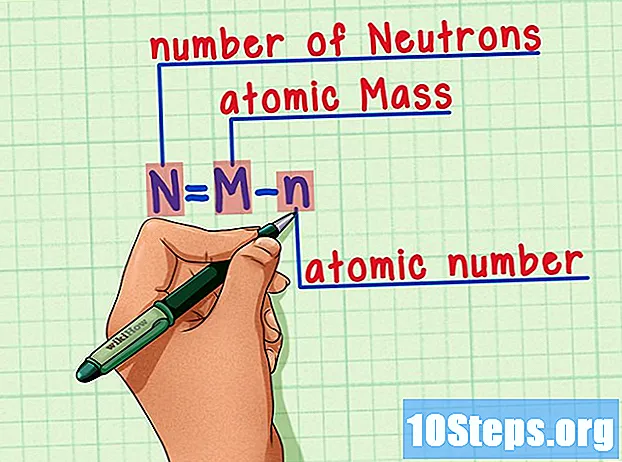
Muista kaava. Käytä seuraavaa kaavaa löytääksesi neutronien määrän tulevaisuudessa: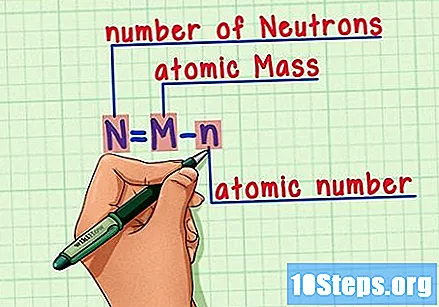
- N = M - n.
- N = lukumäärä Neutrons.
- M = Matomi paisti.
- n = natominen olkaluu.
- N = M - n.
Menetelmä 2/2: neutronien lukumäärän löytäminen isotoopissa
Etsi elementti jaksotaulusta. Otetaan esimerkiksi hiili-14-isotooppi. Koska hiili-14 ei-isotooppinen muoto on yksinkertaisesti hiili (C), etsi tämä elementti jaksotaulukosta (toisesta rivistä).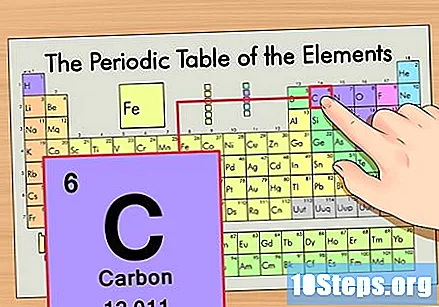
Etsi alkuaineen atominumero. Tämä on yleensä tietyn elementin näkyvin numero ja on yleensä sen symbolin yläpuolella (käyttämässämme taulukossa ei itse asiassa ole muita numeroita). Atomiluku on protonien lukumäärä kyseisen elementin yhdessä atomissa. C on numero 6, mikä tarkoittaa, että hiiliatomilla on 6 protonia.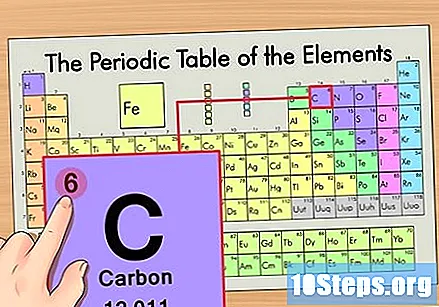
Etsi atomimassa. Tämä on uskomattoman helppoa isotoopeilla, koska ne on nimetty atomimassansa mukaan. Hiili-14: n atomimassa on 14. Kun löydät isotoopin atomimassan, neutronien lukumäärän löytämisprosessi on sama kuin tavallisille atomille.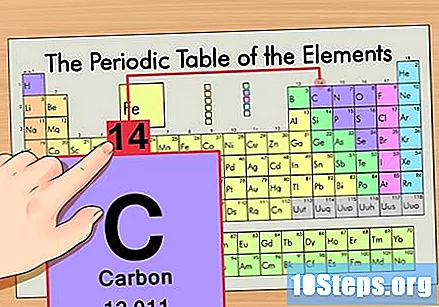
Vähennä atominumero atomimassasta. Koska valtaosa atomin massasta löytyy sen protoneista ja neutraaleista, vähentämällä protonien lukumäärä (eli atominumero) atomimassasta saadaan numero laskettu neutronien määrä atomissa. Desimaalipilkun jälkeinen lukumäärä edustaa yleensä erittäin pientä elektronien massaa atomissa. Esimerkissämme tämä on: 14 (atomimassa) - 6 (protonien lukumäärä) = 8 (neutronien lukumäärä).
Muista kaava. Käytä seuraavaa kaavaa löytääksesi neutronien määrän tulevaisuudessa: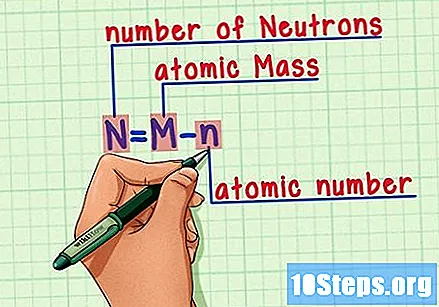
- N = M - n.
- N = lukumäärä Neutrons.
- M = Matomi paisti.
- n = natominen olkaluu.
- N = M - n.
vinkkejä
- Osmium, kiinteä metalli huoneenlämmössä, johtaa nimensä kreikkalaisesta sanasta 'haju', 'osme'.
- Protonit ja neutronit muodostavat lähes koko elementtien painon, kun taas elektronit ja muut monimuotoiset hiukkaset edustavat vähäistä massaa (lähestyy nollamassaa). Koska protoni on suunnilleen sama paino kuin neutraali ja atominumero edustaa protonien lukumäärää, voimme yksinkertaisesti vähentää protonien lukumäärän kokonaismassasta.
- Jos et ole varma, mikä luku on jaksotaulukossa, muista vain, että se tehdään yleensä atominumeron (eli protonien lukumäärän) ympärille, joka alkaa yhdellä (vety) ja nousee yhdellä yksiköllä per vasemmalta oikealle, päättyy numeroon 118 (Ununóctio). Tämä johtuu siitä, että atomin protonien lukumäärä määrää sen, mikä kyseinen atomi on, mikä helpottaa alkuaineominaisuuksien organisointia (esimerkiksi 2 protonin atomi on aina helium, aivan kuten toinen 79 protonin atomi on aina kultaa).